第二類醫(yī)療器械說明書更改告知程序

一����、項目名稱
第二類醫(yī)療器械說明書更改告知
二、受理范圍
省內(nèi)第二類已注冊的醫(yī)療器械����,不屬于注冊變更范圍內(nèi)的說明書其他內(nèi)容發(fā)生變化的書面告知����。
三��、收費依據(jù)
不收費����。
四、辦理條件
由注冊人書面告知��。
五����、資料要求
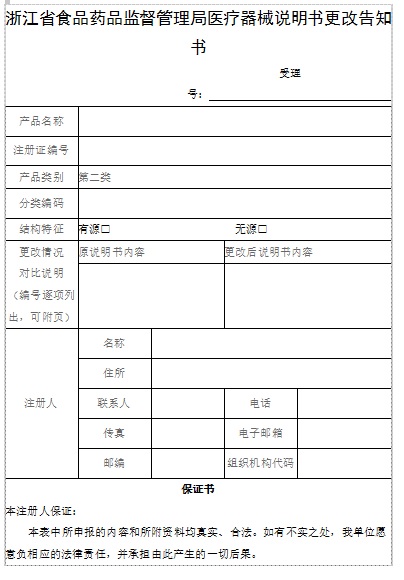
(一)由注冊人簽章的醫(yī)療器械說明書更改告知書��。
(二)說明書更改情況對比說明(含更改情況對比表及變更原因)�。
(三)經(jīng)注冊審查、備案的說明書的復(fù)印件(與原提交審查時核定的產(chǎn)品說明書一致)�����。
(四)更改后的說明書��。
(五)證明性文件:企業(yè)營業(yè)執(zhí)照副本復(fù)印件、組織機構(gòu)代碼證復(fù)印件��、醫(yī)療器械注冊證及醫(yī)療器械注冊變更文件復(fù)印件�,且均應(yīng)在有效期內(nèi)。
(六)具體辦理人應(yīng)提交注冊人或其代理人授權(quán)書及其身份證復(fù)印件���。
(七)注冊人提交的資料真實性的自我保證聲明����,包括所提交資料的清單以及注冊人承擔法律責任的承諾����。
六、辦理程序
(一)浙江省食品藥品監(jiān)督管理局受理大廳對說明書告知資料進行形式審查�����,對于符合要求的�,予以受理。
(二)受理大廳自受理后�����,按程序?qū)⑸暾堎Y料移交省醫(yī)療器械審評中心����。
(三)省醫(yī)療器械審評中心對醫(yī)療器械說明書更改情況進行審核��,審核同意���,則相關(guān)材料按程序歸檔;如不同意�����,則應(yīng)在收到資料后15個工作日內(nèi)告知受理大廳���。
(四)受理大廳依據(jù)醫(yī)療器械審評中心意見�����,在5個工作日內(nèi)制作不予同意通知件,并按程序發(fā)放給申請人��。